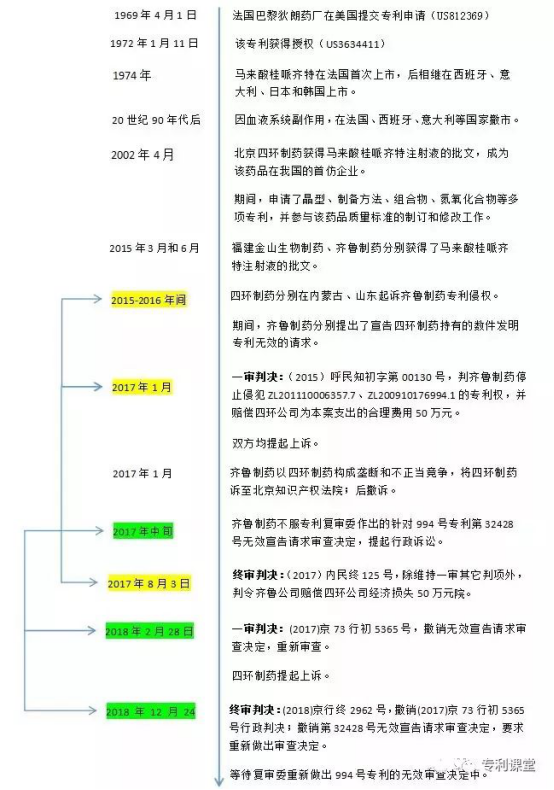
01案情大事记
马来酸桂哌齐特是新一代哌嗪类药物,是心脑血管疾病的一线畅销药,近几年的国内年销售额均达到数亿元。2015年至今,四环制药和齐鲁制药就占领该药市场,硝烟四起,从专利侵权到反垄断,再到专利权无效,剧情不断反转。让我们先来回顾下案件大事记:
02一个杂质化合物专利授权引发的硝烟
从大事记中我们看出,马来酸桂哌齐特因其副作用,已在多国退市。那么,对其副作用的研究和限制,食药总局尤为关注。四环制药首次发现了其中氮氧化物是产生副作用的关键杂质,随后申请专利,并推动了标准修订中对氮氧化物杂质的检测及含量的限制。
四环制药的ZL201110006357.7(简称357号专利),保护含有桂哌齐特和含量不高于0.5%的该氮氧化物杂质的药物组合物;ZL200910176994.1(简称994号专利),保护了该氮氧化物杂质以及作为标准品/对照品的用途。那么,上述两个专利,作为实施马来酸桂哌齐特国家药品标准中无法绕开的专利,就成为了标准必要专利。企业只要生产符合标准的药品,一定会用到该氮氧化物杂质作为标准品,生产出来的产品也必然落入组合物的保护范围。
在众多涉案专利中,994号专利“桂哌齐特氮氧化物、其制备方法和用途”,这个经历了侵权诉讼、无效审查(维持有效)、两次行政诉讼、并且正在等待最新无效审查决定的专利,显得尤为被关注。关于本案,已有多篇文章对994号专利在撰写中“为什么要加入杀虫活性?”“为什么说明书未对杂质相关信息进行说明?”“杂质是否为专利授权客体?”“杂质的新颖性/创造性”“杂质的保护方式”等等问题进行了讨论。虽然,目前导致剧情反转的关键因素是994号专利的化合物杀虫活性等试验数据公开不充分,但纵观整个专利的实审、无效、诉讼过程,无疑暴露了对于杂质化合物各专利审查部门审查标准,尤其在创造性上,不清晰、不一致的问题。
本文希望结合《专利法》、《专利审查指南》,通过审查机构、复审委、法院的观点,来整理分析、专门探讨——杂质化合物创造性的审查标准是什么?
03各审查机构的审查意见
第994号专利有“一种桂哌齐特氮氧化物”、“制备方法”、“用作标准品或对照品的应用”、“杀虫剂组合物”、“用于制备杀虫剂中的应用”5组独立权利要求。在国知局公开专利审查信息中,笔者没有查到994号专利当时的审查意见通知书,但从全A的检索报告来看,当时未对权利要求的创造性进行评述。
为了更好的了解对于杂质化合物,专利实质审查部门的审查标准。笔者在专利检索系统SOOIP中,对中国专利进行检索,筛选出权利要求中涉及保护“杂质化合物及其标准品/对照品用途”的已结案专利45项进行分析。所分析专利的审查分布在国知局和各地审协,其中,审协北京中心和江苏中心结案10件以上,国知局、广东中心、天津中心、湖北中心、河南中心不足5件。结案年份在2010-2018年间,并主要集中在近3年(2016-2018年,结案24件),较能代表近年来的审查标准,分析结果如下:
(一)关于说明书
考虑到说明书对解释权利要求的重要性,我们先对上述专利说明书记载的内容做以总结。
上述大部分专利在说明书背景技术中会提及杂质会直接影响药品的质量、安全性和疗效,对杂质化合物研究,可以提高活性化合物纯度,并进一步提高产品的质量标准;发明人发现了前所未报道的新杂质化合物,并在发明内容中给出了杂质的制备和检测方法。
仅有3项专利提及杂质具有潜在的基因毒性(CN201610203513.1一种西地那非杂质F及其制备方法和应用)或会引起过敏反应(CN201310733125.0用于马来酸氟吡汀分析中的参比化合物、CN200710307231.7比阿培南二聚物及其制备方法),但并未给出具体的毒性试验数据;
有1项专利给出杂质化合物具有杀螨活性(CN201110178880.8一种氟吡汀偶联物及其制备方法和用途),并给出实验数据。
有个别专利给出了杂质的分离方法,以及降低杂质含量的工艺改进方法,可控制更低的杂质含量(CN201010272773.7硝苯地平的制备及其杂质分离方法与应用、CN201310643492.1化合物对甲基苯甲酸4-(2-二甲胺基-1-环己烯基乙基)苯酯制备方法及应用)。
综上,所有专利都指出要求保护的化合物为药物中新发现的杂质,并公开了新化合物的制备和鉴定,但对于新化合物确为药物杂质的证明、新杂质的含量或杂质的副作用证明等,几乎均未在说明书中记载。
(二)授权倾向
45项专利中,有权38项,无权7项。
在38项有权的专利中,24项专利的化合物权利要求授权,14项专利在删除化合物权利要求后(大部分因化合物涉及新颖性问题而删除,3项专利因创造性问题删除),其制备方法和/或用途权利要求获得授权;
在7项无权的专利中,3项驳回(1项因化合物创造性问题驳回,2项涉及化合物缺乏新颖性,方法和用途缺乏创造性驳回),3项撤回,1项因未缴纳年费专利权终止。
可见,新杂质化合物的专利,在其化合物具备新颖性的情况下,无论其化合物权利要求、还是方法、用途权利要求,均有较高的授权率。
(三)创造性评述理由
审查意见通知书中,针对杂质化合物创造性的评述理由,主要有以下几种:
1. 相似化合物的结构改造容易想到,对照品的应用为常规,杂质化合物不具备创造性。
审查意见简述:以公开结构相近的化合物文献为最接近的现有技术。杂质化合物与现有技术化合物结构相似,实际解决的技术问题是提供类似的化合物;而新化合物是通过在现有技术的基础上进行结构改造容易想到的,因此不具备创造性。
相关案例:
CN201510745121.3一种醋酸乌立妥原料药杂质及其制备方法和作为标准品的用途;
CN201410512926.9一种雌酚酮原料药杂质及其制备方法和作为标准品的用途。
案件经过:杂质并没有所述活性,发明人并不具有在已知活性化合物基础上,进行结构修饰的动机。而审查意见单纯从结构出发,以“结构改造容易想到”为由,忽略发明人的动机和化合物的效果,过于“事后诸葛亮”。自然,在申请人一通答复后,杂质化合物及其制备方法、用途均获得授权。
2. 杂质化合物的发生容易想到,且对照品的应用为常规,杂质化合物不具备创造性。
审查意见简述:以公开药物的制备及其杂质的文献作为最接近的现有技术。实际解决的技术问题是提供更多的可用于药物质量检测的杂质化合物。本领域技术已知,药物杂质的来源一般分为从原料中引入、生产过程入和在储存过程中产生。在对比文件的基础上,根据反应原料、反应路线等,结合公知常识,可以预期产生本申请要求保护的杂质化合物。在此基础上,对于本领域技术人员而言,为了控制产品质量,有动机分析以及制备反应中产生的杂质,并将其用作对照品,分析产品杂质含量。
相关案例:
CN201310733125.0,用于马来酸氟吡汀分析中的参比化合物
CN201210277120.7,化合物5,6,7,8-四氢-6-[N,N-二[(2-噻吩)乙基]]氨基-1-萘酚、制备方法及应用
CN201610203513.1,一种西地那非杂质F及其制备方法和应用
案件经过:申请人往往从“化合物和制剂中杂质的确定及控制是非常复杂的过程,化合物和制剂在生产、储存、使用过程中都有可能产生杂质,其杂质的化学结构具有不可预知性”的角度进行答复,使得随后获得授权,即大部分杂质化合物的权利要求均也获得授权;也有个别杂质可预期很强的案件走向驳回(例如:CN201210235493.8一种左氧氟沙星杂质的制备方法)。
3. 杂质化合物的对照品用途如未产生预料不到的技术效果,杂质化合物不具备创造性。
审查意见简述:药物的活性成分不可能达到100%纯净,往往含有多种不同的杂质,但并不是所有的杂质都必须除去。在说明书未记载任何有关去除杂质能够给药物在产品质量、安全性及合成工艺上带来任何预料不到的技术效果,而是简单分离并鉴定了对产品质量影响非常有限的新杂质,这种分离鉴定对本领域技术人员来说是的公知常识,看不出将这些杂质分离鉴定出来对实际生产有任何意义。
相关案例:
CN201410155967.7,一种厄洛替尼的新杂质及其制备方法
CN201310711981.6,一种吉非替尼的新杂质及其制备方法
案件经过:在申请人删除化合物及其应用的权利要求,仅保留方法权利要求的情况下,专利获得授权。
(四)创造性评判标准
综上,针对新的杂质化合物,各审查部门对创造性的评述理由不尽相同。结合申请人的答复和最终的授权结果来看,可以得出两个不同的评判标准:
审查标准1:一个杂质化合物,如能毫无疑义的预期产生,将其作为药品的标准品/对照品为公知常识,该杂质化合物不具备创造性,除非该化合物具备其他预料不到的技术效果;如不能毫无疑义的预期产生,发明人发现该杂质,并可将其作为某药品的标准品/对照品,则该杂质化合物具备创造性。
审查标准2:一个杂质化合物如不能给药物在产品质量、安全性及合成工艺上带来预料不到的技术效果,则该杂质化合物及其作为标准品/对照品的用途不具备创造性。
回到994专利,我们再来看一下复审委和法院的观点。
04复审委审查意见
1. 复审委(第32428号)
复审委在针对杂质化合物的创造性问题,指出“本专利实际解决的技术问题是发现了式(I)的桂哌齐特氮氧化物并确定了其结构,及其用作标准品或对照品,和作为杀虫活性化合物的用途”。
主要评述理由:
(1)在没有证据证明桂哌齐特中可能存在氧化物杂质及其种类、结构的情况下:
本领域技术人员尚未认知到药物产品中具体含有何种杂质,哪些杂质是具有强烈生物作用或毒性的,哪些杂质是可以不对其进行特殊控制的前提下,本领域技术人员不会有启示对其进行有意识地分离、纯化和表征。没有动机对其进行研究,进而制定相应的质量标准,也不能预期该化合物具备何种用途;
在药物化合物领域,杂质来源是多种多样的,在本领域技术人员尚未能了解某特定杂质的任何相关信息时,且尽管有多种现代化分离和检测手段,仍然难以有效地针对特定杂质进行检测、分离和鉴定,进而对药品质量进行更为精确的控制。
注:笔者不赞同复审委该观点,判断技术方案是否具备创造性的实质是其是否对现有技术做出了贡献,解决了技术问题,而与技术方案获得的难易没有直接的必然联系。
(2)在有证据能够判断桂哌齐特化合物能够产生氮氧化物的情况下:
桂哌齐特在何种条件下氧化、氧化究竟发生在哪个位置,上述证据并未涉及,不能仅根据理论上的可能性就直接地、毫无疑义地认定产生本申请所要求保护的氮氧化物,更无从获知其还具备杀虫作用。
分析来看,复审委的观点基本与上述“审查标准1”一致:如果能够毫无疑义的预期产生某杂质,需要该杂质具备预料不到的技术效果(如杀虫);如果不能预期产生某杂质,则检测、分离和鉴定,发现该新的杂质化合物为无动机的研究,进而发现该化合物可以控制药品的质量的用途,具备创造性。
05法院观点
1. 一审法院((2017)京73行初5365号)
一审法院参考《审查指南》对于“结构上与已知化合物接近的化合物,必须要有预料不到的用途或效果”的要求。
主要评述理由是:
要求保护的化合物是桂哌齐特中一个N原子被氧化得到,对比二者的结构式可知二者属于结构相近的化合物。因此,必须要有预料不到的用途或效果。但本专利说明书中的实验数据不足以证明本专利要求保护的化合物具有杀虫活性,即现有证据不能证明杂质化合物相对于已知化合物桂派齐特,具有预料不到的用途或效果。
总结一审法院的观点:杂质化合物如与现有技术结构相近,需要具备预料不到的技术效果(如杀虫)方具有创造性。即一审法院认为单纯作为标准品/对照品的用途不属于预料不到的技术效果。
当然,笔者认为,一审法院参考《审查指南》针对具备相似结构且无预料不到效果化合物的评述逻辑,不能当然适用于杂质化合物。因为这里的“预料”是指“预料”和相似结构化合物有相似的效果,而杂质并没有相似活性,更确切的说并未发现有任何活性。
2. 二审法院((2018)京行终2962号)
二审法院针对创造性的主要理由是:
本专利要求保护桂哌齐特的氮氧化物与各对比文件相比,区别在于明确了桂哌齐特氮氧化物的结构。本专利要求保护的化合物要具备创造性,必须要有预料不到的用途或效果。而桂哌齐特氮氧化物具有作为标准品/对照品的应用的用途,能够证明该技术方案具有的一个技术效果,即相对于对比文件所公开的桂哌齐特或其盐而言,具有预料不到的技术效果。
二审法院的观点:杂质化合物的标准品/对照品用途属于预料不到的技术效果,杂质化合物具有创造性。
二审法院直接认定“专利要求保护的化合物要具备创造性,必须要有预料不到的用途或效果”,以及“能够证明该技术方案具有的一个技术效果”即预料不到的技术效果,缺乏说理,不够完善。
06问题引出
将上述标准、观点中的问题总结一下,对于杂质化合物,各种不一致,创造性争议的焦点在于:
1. 如何考虑杂质化合物容易预期产生?可预期的程度要求有多高?——是有可能产生?还是毫无疑义会产生呢?
2. 如何判定杂质化合物预料不到的技术效果?——作为标准品/对照品用途?还是发现其副作用?还是发现其完全不相关的活性?
上述问题是对发明创造性评判中非常重要的内容。然而,笔者认为——所有抛开来源、含量以及安全性讨论杂质的,都是耍流氓!
对于杂质化合物而言,除了“审查标准2”略有涉及外,其余都忽略了一个非常最重要的问题:
杂质化合物研究,要解决的技术问题是什么?
(未完待续——关于该问题的分析请见下篇文章)
来源:《SOOIP大数据》