氟虫腈(fipronil)是1986年由罗纳-普朗克公司(曾与赫斯特公司的农业部门合并,成立了安万特公司,后又被拜耳收购)开发的苯基吡唑类杀虫剂,氟虫腈具有活性高、持效期长、杀虫谱广、对作物安全性高等特点,对半翅目、同翅目、双翅目、直翅目、鳞翅目、缨翅目、鞘翅目等害虫都有很高的防效,同时对许多病菌(如腐霉菌、白叶枯病菌)均有抑制作用,并能促进植物生长。作为农药发展史上最经典的农药之一,氟虫腈曾在农业生产中为全球种植者带来了显著的增产效果。但由于氟虫腈及其代谢产物对环境的毒性较高,氟虫腈在各个国家相继被禁用,2009年我国停止销售和使用。虽然后来上市的康宽、溴虫腈弥补了一部分氟虫腈的市场空缺,但氟虫腈的禁用仍旧成为很多企业或种植者心中的“意难平”,也因而围绕氟虫腈的研发探索一直未间断,像乙虫腈、丁虫腈、乙酰虫腈、吡啶唑虫胺、吡唑虫啶、氟吡唑虫、唑虫烟酰胺、Fiprl-1等,由于毒性、防效、合规等原因这些化合物目前都没有能在重现像氟虫腈一样的辉煌。
01 产品简介
英文名称:fipronil
中文名称:氟虫腈
其他名称:锐劲特;氟苯唑;芬普尼
化学名称:rac-5-氨基-1-[2,6-二氯-4-(三氟甲基)苯基]-4-[(R)-三氟甲基亚磺酰基]吡唑-3-腈
分子式:C12 H4 Cl2 F6 N4 O S
相对分子质量:437.148
CAS登录号:120068-37-3
结构式:
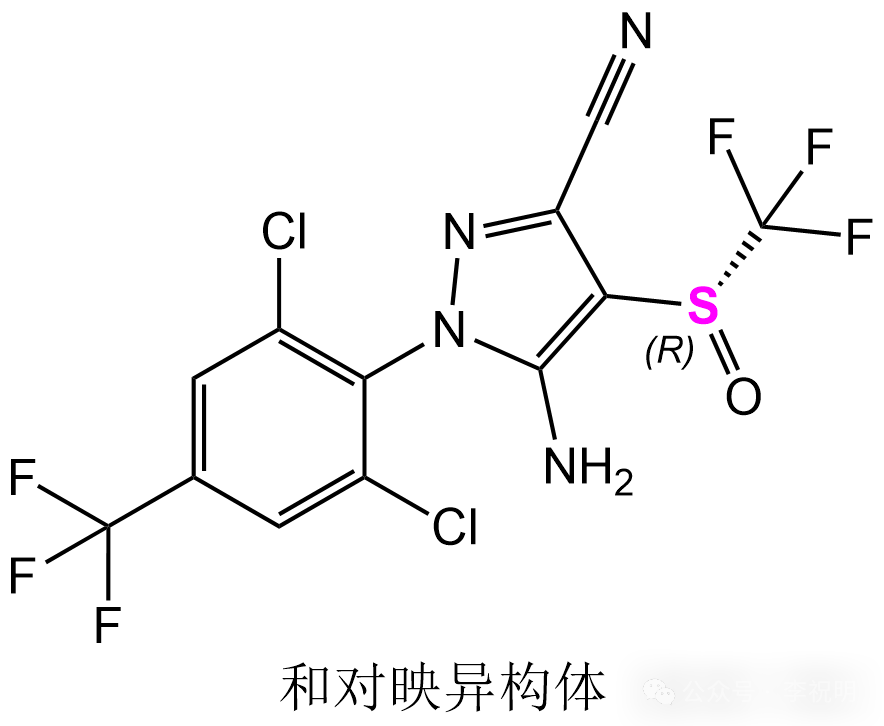
三维结构式:
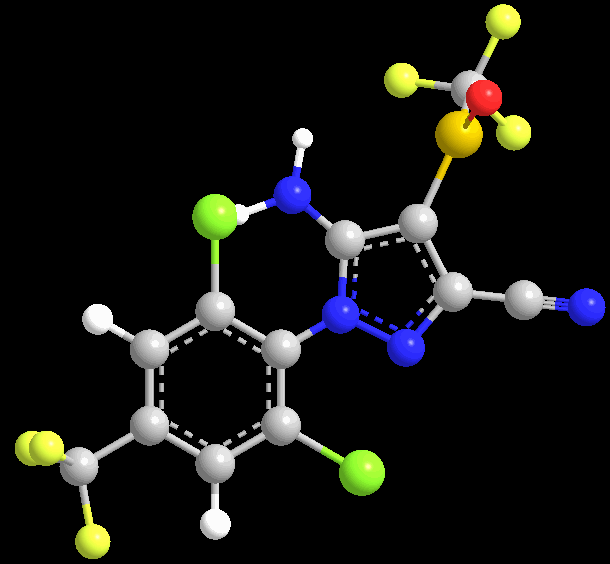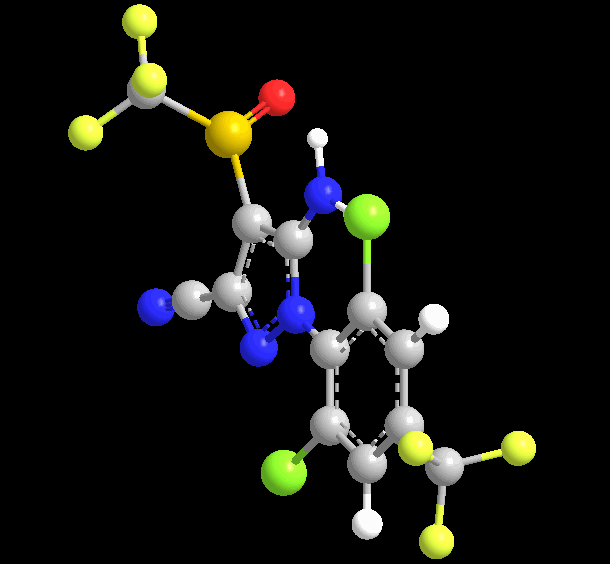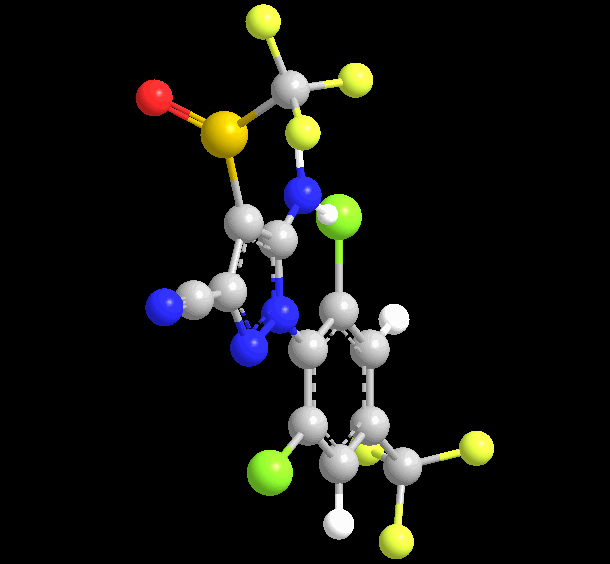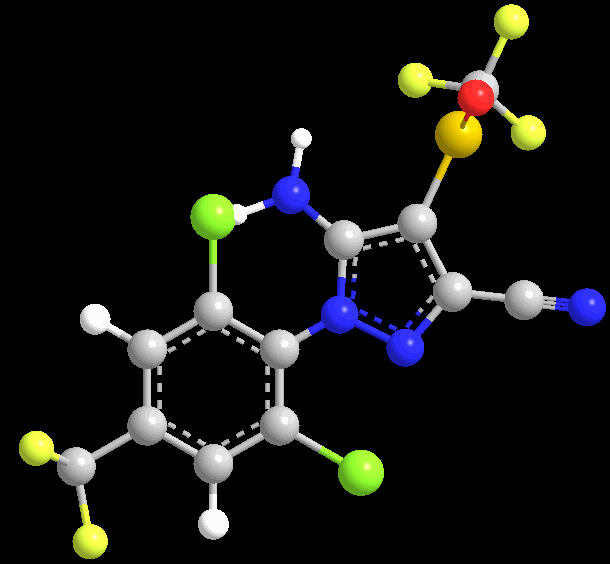
理化性质:原药为白色固体,熔点200~201℃,密度1.477~1.626(20℃)。蒸气压3.7x10-7pa(20℃):分配系数(25℃)logP=4.0。水中溶解度(20℃,mg/L)1.9(蒸馏水),1.9(pH=5),2.4(pH=9);其它溶剂中溶解度(20℃,g/L):丙酮545.9,二氯甲烷22.3,甲苯3.0,己烷<0.028。在pH=5、7的水中稳定,在pH=9 时缓慢水解,DT50约为28天,在太阳光照下缓慢降解,但在水溶液中经光照可快速分解。
氟虫腈属于γ-氨基丁酸(GABA)门控氯离子通道阻滞剂,作用于昆虫神经系统。通过阻断GABA激活的氯离子通道,从而引起昆虫过度兴奋和惊厥。GABA是昆虫神经兴奋传导中主要的抑制性神经递质。
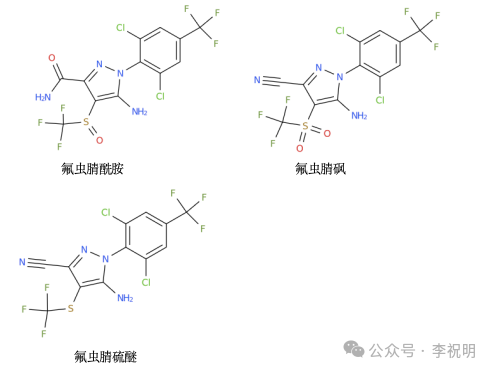
毒性:实验室及田间实验表明,在不同温度、不同土壤类型条件下,氟虫腈的代谢产物共有五种:RPA200766(酰胺),MB46513(脱亚砜基氟虫腈),RPA104615(吡唑-4-磺酸),MB46136(砜),MB45950(硫醚)。其中部分代谢产物的毒性要高于氟虫腈本体,如脱亚砜基氟虫腈毒性是氟虫腈本体的9倍,氟虫腈砜的毒性是本体的6倍,所以最早的时候一些不良厂家将氟虫腈氧化成“砜”之后当所谓“特效黑科技”售卖,虽然对抗性蓟马特效,但其对环境如脊椎动物、部分水生生物、部分鸟类、啮齿类动物等造成的危害不可估量,同时值得注意的是,氟虫腈还具有遗传毒性,父母长期接触氟虫腈砜后血清中的氟虫腈可转移给胎儿,对婴儿健康结果产生不利影响。所以一定程度上监管部分的懒政与犯罪无二。
03 应用
应用作物:水稻、玉米、棉花、香蕉、甜菜、马铃薯、花生、甘蔗、果树、桑树等,以及蚊、蝇、白蚁等公共卫生领域或兽药。
防治害虫:鳞翅目(青虫、肉虫)、同翅目(蚜虫、飞虱)、半翅目(椿象)、缨翅目(蓟马)、双翅目(蚊、蝇)和直翅目(蝗虫、蟋蟀、蝼蛄)及鞘翅目(叶甲)等
开发剂型:50g/L氟虫腈悬浮剂、80%氟虫腈水分散粒剂、4g/L氟虫腈超低容量剂、50g/L氟虫腈悬浮种衣剂、0.3%氟虫腈颗粒剂、0.1%氟虫腈粉剂
04 专利情况
1986年罗纳-普朗克公司在全球31个国家和地区申请了基于氟虫腈在内的N-苯基吡唑类的化合物专利。
专利名称:应用N-苯基吡唑类杀虫的方法
申请号:CN86108643.0
授权日:1994/09/07
申请日:1986/12/19
失效日:2001/12/19
其他国家专利:GB8531485D0、MY100259A 、CA1311242C、KR870006005A、EP0579280A1、JPS62228065A、DE3650490D1、RU2080789C1、WO8703781A1
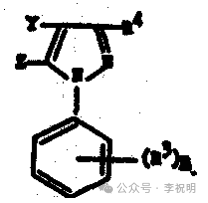
摘要:本发明提供使用下式化合物或其盐类防治节肢动物、植物线虫或蠕虫虫害的方法,并描述了杀虫剂组合物、新化合物及其制备方法。下式中各取代基的定义如说明书中所述。
05 合成路线
目前合成氟虫腈的路线主要有三条,反应都涉及关键中间体5-氨基-3-氰基-1-(2,6-二氯-4-三氟甲基苯基)吡唑(吡唑环、芳基吡唑腈)。
路线1:最早的专利EP295117、EP0374061等报道了由5-氨基-3-基-1-(2,6-二氯-4-三氟甲基苯基)吡唑与三氟甲硫基卤代烷反应,引入三氟甲硫基,再经间氯过氧苯甲酸氧化而得到氟虫腈。合成路线如下:
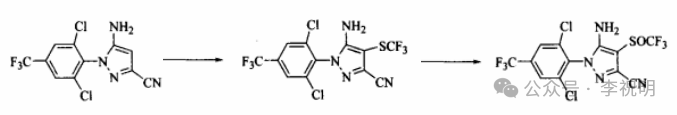
由于CF₃SX的毒性均极高,且实验采用的CF₃SCl为气体,因此,操作过程中要十分注意安全问题。其次,由于采用间氯过氧苯甲酸作氧化剂,氧化时间一般需2d甚至更长,而反应时间过长会导致副产物增多,产率低且间氯过氧苯甲酸价格较高,因而不适用于大规模工业生产。
路线2:专利WO0059862报到了由5-氨基-3-基-1-(2,6-二氯-4-三氟甲基苯基)吡唑先制备双硫代物,用卤代烷经三氟乙酸/过氧化氢氧化得到氟虫腈。合成路线如下:
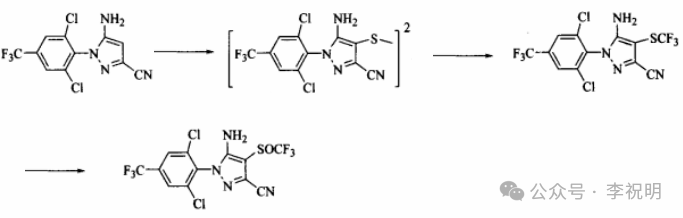
路线二采用先形成双硫代物后用毒性较小的卤代烷CF₃Br断键形成CF₃S-R,减少了路线一中CF₃S-X的高毒性问题,同时采用CF₃COOH/H₂0₂的混合物作氧化剂同时加入硼酸作为防腐蚀剂,在选择性和产率上均达到了很好的效果,适合工业化生产。
路线3:专利US4096185、US6133432、EP668269等报道了由5-氨基-3-氰基-1-(2,6-二氯-4-三氟甲基苯基)吡唑与亚磺酰基取代物反应一步合成得到氟虫腈。合成路线如下:
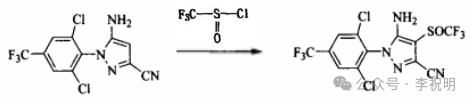
路线三路线短,避免了使用高毒的CF₃SX,同时避免了氧化反应,减少了副产物,也适合工业化生产。
中间体吡唑环的制备
目前制备吡唑环的成熟路线主要有2条,
路线一:专利WO9306389、US5232940等专利报到了以2,6-二氯 -4-三氟甲基苯胺为原料,以硫酸为反应介质,滴加亚硝酸钠的水溶液进行重氮化反应,重氮化反应液在一定温度下,加入2,3-二氰基丙酸乙酯,在弱碱性条件下于有机溶剂中进行环化反应,反应结束后经后处理得到95%含量的吡唑环。反应路线如下:
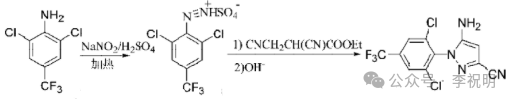
路线二(肼路线):专利US6084105报道了以2,6-二氯-4-三氟甲基苯肼与丁二腈(富马腈)反应,后经氧化、关环得到93%含量的吡唑环。合成路线如下:
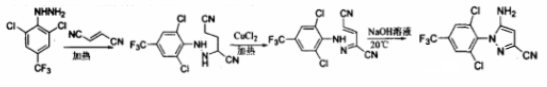
06 产品评价
目前氟虫腈在全球主要国家都已经进行限用。这是一个基于公共利益、环境保护和农业可持续发展等方面经过综合科学评估得到的结果。从长远看,是利大于弊的明智之举。
抛开对环境和非靶标生物以及人类健康的风险来讲,氟虫腈可以说是目前开发最成功最优秀的化合物没有之一。即使氟虫腈已经禁用了20多年,可围绕氟虫腈所做的研究截至目前从未停止,大连九信、广西田园、拜耳、日本三菱、日本农药等国内外企业一直在做相关研究,并有部分化合物也成功上市,如丁虫腈、乙虫腈等,但这些化合物都是围绕氟虫腈本体结构进行修饰的,要么防效不理想,要么毒性高难能商业化,后来的“康宽”、“除尽”、“安打”虽然被作为氟虫腈的替代品在市场上销售,但其广谱性、速效性和耐抗性远远比不上氟虫腈。直到后来的同作用机理的异噁唑啉类化合物的上市,才让完全替代并超越氟虫腈有望成为可能。
虽然氟虫腈农业上基本被限制使用,但其在室外消杀、公共卫生领域、兽药(驱杀犬、猫体表的跳蚤和虱子,对狗、猫安全),旱田种子包衣等方面仍旧是最具性价比的产品。且围绕氟虫腈在农业害虫的防治方面的研发也会一直持续。