20世纪90年代, 对羟基苯丙酮酸双加氧酶(4-hy-droxyphenylpyruvate dioxygenase, HPPD)首次被确定为除草剂作用靶标.以HPPD为靶标的除草剂具有高效、低毒、作物安全性高、不易产生抗性、环境相容性好以及对后茬作物安全等一系列优点[1]. HPPD是生物体内酪氨酸代谢过程中重要的酶, 它几乎存在于所有需氧生物体内.生物体内酪氨酸(Tyrosine)在酪氨酸氨基转移酶(Tyrosine aminotransferase, TAT)的作用下生成对羟基苯丙酮酸(p-hydroxyphenylpyruvic acid, HPPA), 在氧气的参与下HPPD能够将HPPA催化转化成尿黑酸(HGA).在植物体内, 尿黑酸(HGA)能够被进一步转化成质体醌和生育酚[2].生育酚是植物体内重要的抗氧化物质, 能有效地增强植物的抗逆性.质体醌是植物进行光合作用过程中关键的辅助因子, 促进植物体内类胡萝卜素等的合成.在植物体中高于60%的叶绿素都结合于捕光天线复合物上, 该复合物吸收太阳光能并将激发能传递给光合作用反应中心, 而类胡萝卜素是反应中心的叶绿素结合蛋白和天线系统的重要组成部分, 在植物光合作用中担负着光吸收辅助色素的重要功能, 具有吸收和传递电子的能力, 并在清除自由基方面起着重要的作用.因此, 一旦HPPD的活性被抑制, 植物体内酪氨酸正常代谢将被阻断, 导致在植物体内类胡萝卜素的缺乏, 从而诱导叶绿素光氧化作用减弱, 影响植物的光合作用, 促使植物产生白化症状而死亡[3~7].
结合最新的研究进展, 本文对目前已经报道的不同种属来源的HPPD的晶体结构、抑制剂小分子与靶标酶的结合模式及其在植物体内的代谢产物进行系统的总结, 同时对不同商品化吡唑类HPPD除草剂的优缺点进行对比分析, 并对这类除草剂的发展方向进行了介绍.
HPPD的结构、活性位点及其可能催化机理1.1 HPPD的结构及活性位点
HPPD抑制剂作为除草剂的使用历史可以追溯到20世纪80年代初, 1980年日本三共制药有限公司首次将吡唑特投入到世界除草剂市场.当时并不知道吡唑特的作用靶标就是HPPD. HPPD真正被确定为除草剂作用的靶标是从20世纪90年代开始.随后, 人们不断地从老鼠[8]、猪[9]、兔[10]以及人的肝脏[11]、玉米[12]、胡萝卜[13]、拟南芥[14]、荧光假单胞菌[15]和链霉素[16]等体内提取或克隆HPPD.目前, 文献上已经报道的主要有14个HPPD或其复合物的晶体结构, 其中有12个晶体结构已经被蛋白质数据库(PDB)收录, 详细信息见表 1.拟南芥是植物界里面一个具有代表性的模式生物, 因此关于HPPD的晶体结构报道的最多的是拟南芥源HPPD (AtHPPD).其中大部分晶体结构是以二聚体的形式存在的。
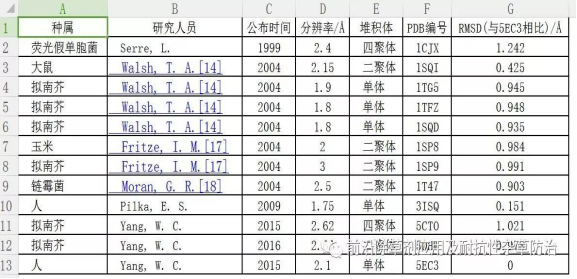
表 1 已经公布的HPPD的晶体结构信息
Table 1. Announced HPPD crystal structure information
对比分析拟南芥源和人源的HPPD晶体结构[24](图 1)可以看出, 来自拟南芥源HPPD (AtHPPD)和人源HPPD (hHPPD)晶体结构具有高度的相似性, 每个单体都是由具有相似的拓扑结构域组成, 都存在着一种α/β折叠方式, 该折叠是由一个平行的和反平行的β链围绕着一个α螺旋所组成的结构.其活性位点位于一个扭曲打开的β折叠区, 由7个β折叠构成.在活性空腔内, 具有催化活性的Fe2+以六配位的形态存在, 与相邻的高度保守的氨基酸残基(一个谷氨酸和两个组氨酸)及一分子游离的水形成配位作用, 并和底物HPPA分子中的两个氧原子形成双齿螯合型配位键, 进而形成一个稳定的八面体结构, 发挥其生物催化功能.随后人们对于不同种属来源的HPPD的差异性也进行了深入研究.
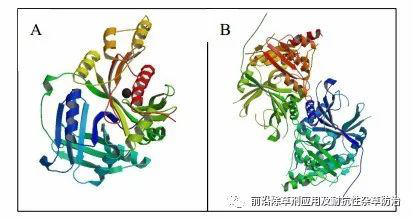
图1hHPPD晶体结构(A, 2.1 Å)和AtHPPD与抑制剂的共晶体结构(B, 2.62Å) Figure1.Crystal structure of hHPPD (A, 2.1Å) and crystal structure of inhibitor with AtHPPD (B, 2.62 Å)
2004年Walsh[14]及2013年Richard和Jane等[19]分别对不同种属来源的HPPD进行结构比对分析(表 2).通过对比分析, 植物与哺乳动物的HPPD氨基酸序列的同源性存在显著的差异性, 而同为植物界或者动物界的同源性比较高.哺乳纲的人和老鼠的氨基酸序列的同源性高达90%.同时, 在HPPD的活性空腔内, 对其52个具有生物活性的氨基酸残基位点进行对比分析, AtHPPD与哺乳纲的人、小鼠及猪的活性位点差异个数为13~14个, 而同为哺乳纲的人、小鼠及猪的活性位点的氨基酸残基差异个数只有1~2个.因此, 为后续开发具有高选择性、安全性的HPPD类除草剂提供了理论指导基础.
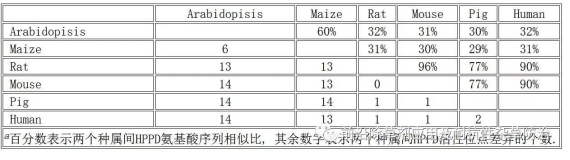
表 2 不同种属来源的HPPD氨基酸序列比对aTable 2. Different species of HPPD amino acid sequence alignment
结合计算化学方法[20], 分别选取AtHPPD (PDB编号: 1SQD), RnHPPD (PDB编号: 1SQI)以及hHPPD (PDB编号: 3ISQ)的晶体结构, 以HPPD催化中心Fe2+周围12 Å范围内的氨基酸作为活性位点的考虑范围进行序列比对(图 2).结果表明hHPPD与RnHPPD的活性腔序列相似性高达97%, AtHPPD与hHPPD和RnHPPD相比, 活性腔序列相似性都为66%, 图中虚线框中的氨基酸为催化中心Fe2+周围12 Å范围内的氨基酸残基, 灰色代表在三类种属HPPD活性腔中有差异的氨基酸残基位点, 共17个, 但是其中只有两个位点的氨基酸残基Met314和Lys400(以拟南芥1SQD为标准)是在结合位点附近, 通过序列比对其在RnHPPD (PDB ID: 1SQI)中的等位残基分别为Leu289和Ala361, 在hHPPD (PDB ID: 3ISQ)中的等位残基分别为不同种属来源的HPPD其活性位点氨基酸残基具有一定Leu289和Ala361.从氨基酸序列比对的结果分析, 的差异性.其可能会影响抑制剂与HPPD结合的稳定性, 导致抑制剂分子在不同种属来源的HPPD抑制活性的不同, 为后续设计选择性好、安全性高的抑制剂提供理论基础.

图2AtHPPD, hHPPD和RnHPPD催化中心的氨基酸序列比对 Figure2.Sequence alignment of the amino acids in the active sites of AtHPPD, hHPPD and RnHPPD
1.2 HPPD的可能催化机理
文献上已经报道了多种植物体内HPPD催化HPPA生成HGA的这一生物反应机制[21~23], 而普遍接受的是如Scheme 1所示的催化反应机理[24~27].
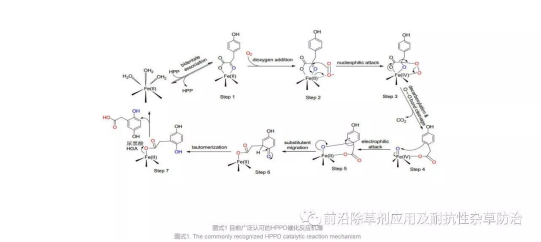
图式1目前广泛认可的HPPD催化反应机理
Scheme1.The commonly recognized HPPD catalytic reaction mechanism
该机理包括羰基的脱除反应、芳香环的羟基化和取代基的迁移反应.在催化反应进行的时候, HPPA首先与HPPD的催化活性中心Fe2+进行配位形成一个六配位过渡态(step 1), 紧接着一分子氧插入到该过渡态中, 二价铁随后被氧化成了四价铁形成了过渡态(step 3).经过O—O键的断裂以及二氧化碳的脱除反应得到过渡态(step 4), step 4结构中的苯环是一个富电子的官能团, 它进攻高价铁中的氧原子形成step 5.四价铁随后被还原成二价铁, 再经过烷基的迁移反应、烯醇互变反应得到过渡态(step 7), step 7脱除尿黑酸完成了整个催化反应循环.在完成一个催化反应循环后, HPPD又继续进行下一个催化反应过程, 所得到的尿黑酸进入后续的生理转换过程中.
2 吡唑类HPPD除草剂的作用模式及研究历程2.1 吡唑类HPPD除草剂的作用模式
HPPD广泛存在于自然界的各种需氧生物体中.从催化中心的结构上来讲, HPPD属于2-组氨酸-1-羧酸盐面三联体结构氧化酶大家族中的一员, 从在细胞中的位置上来讲, HPPD又属于细胞质酶.近年来人们也培养出了一些商品化的抑制剂与AtHPPD复合物的晶体结构. 2008年拜耳公司报道了磺酰草吡唑与AtHPPD复合物单晶[28].从所得到的AtHPPD-磺酰草吡唑复合晶体结构分析, 磺酰草吡唑与AtHPPD的结合力主要受两个方面的因素控制:一方面是磺酰草吡唑分子中的氧与二价铁之间的螯合作用力, 另一方面是磺酰草吡唑分子中的疏水基团与催化口袋之间的疏水作用力.
HPPD催化活性中心位于一个开口扭曲的螺旋状的β结构中, 该结构是由7个β折叠组成.晶体的每一个单体中都含有一个二价铁离子, 二价铁是以六配位的形式存在的, 其中2个组氨酸、一个谷氨酸以及一个水分子各占据一个配位键, 抑制剂分子中苯甲酰乙烯片段的2个氧原子各自与Fe2+形成一个配位键(图 3).磺酰草吡唑分子中N上的甲基朝向一个疏水性的小口袋之中, 这个口袋很小说明在吡唑环上不能引入体积过大的基团.磺酰草吡唑分子中的苯环结构能够与周围的2个苯丙氨酸形成三明治型的π-π堆积作用.由于苯环上间位的三氟甲基结构与周围疏水性氨基酸残基的距离小于4 Å, 它们之间会存在一个疏水相互作用力.在实验的过程中人们也发现AtHPPD中C-端螺旋结构会呈现出开关构象, 当处于开放的构象时则有利于底物进入到催化位点以及产物的释放; 而处于闭合的构象时则有利于保护催化反应免受溶剂的影响.
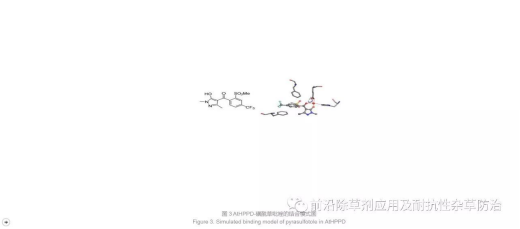
图3AtHPPD-磺酰草吡唑的结合模式图
Figure3.Simulated binding model of pyrasulfotole in AtHPPD
2.2 商品化的吡唑类HPPD除草剂
HPPD是继乙酰辅酶A羧化酶(ACCase)、乙酰乳酸合成酶(ALS)后的又一重要的除草剂作用靶标.由于其独特的作用机制可以有效防治多种抗性杂草.商品化的HPPD除草剂主要分为三酮类、吡唑类、异噁唑类(二酮腈).三酮类和异噁唑类已有相关的文献报道. 2016年新上市的HPPD除草剂环吡氟草酮和双唑草酮都属于吡唑类, 因此主要对吡唑类HPPD除草剂的研究现状进行总结.
20个世纪70年代, 日本三共制药公司报道了苄草唑(Pyrazolynate), 商品名为“Sanbird”.主要用于水稻田, 在3~4 kg ai/ha的剂量下对一年生或多年生的杂草具有较好的防效.苄草唑作为一种前药, 在水中分解释放出具有生物活性分子.通过植物的吸收传导, 到达作用靶点进而发挥药效.苄草唑在水中的半衰期与温度和pH相关, 尤其是在偏碱性的水中半衰期只有4.3 h (T=25 ℃), 在土壤中的降解时间DT50=8~10 d, 因此严重制约了苄草唑的药效.苄草唑的合成路线如Scheme 2所示, 2, 4-二氯苯甲酰酰氯Ⅱ-1b和吡唑醇Ⅱ-1a在Ca(OH)2作碱及异丙醇作溶剂的条件下得到化合物Ⅱ-1c. Ⅱ-1c再与对甲苯磺酰氯反应即能制备苄草唑.该合成路线便捷, 合成成本低廉, 在初期也有非常好的市场价值.
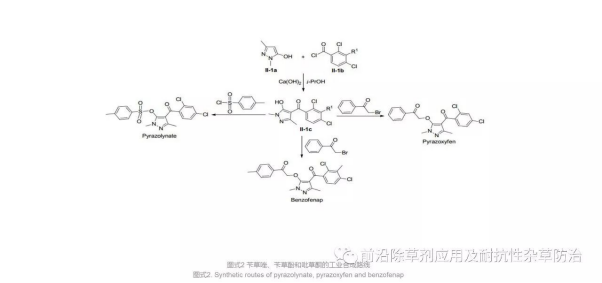
图式2苄草唑、苄草酚和吡草酮的工业合成路线
Scheme2.Synthetic routes of pyrazolynate, pyrazoxyfen and benzofenap
1984年, Kimura[29]首次报道了苄草酚(Pyrazoxyfen). 1985年, 日本石原产业株式会社正式将苄草酚推向市场, 商品名为“Paicer”.同样适用于水稻田, 在推荐剂量3 kg ai/ha下, 对灌溉田的阔叶杂草具有较宽的杀草谱.然而, 苄草酚对水稻的安全性受温度的影响.当气温低于35 ℃时, 对于移栽稻田和直播稻田的水稻不会产生毒副作用; 当气温高于35 ℃时, 则会对水稻产生短暂性药物毒性, 因此其在推广过程中受到了严重的限制.其合成路线与苄草唑类似(Scheme 2).
1987年, 日本三菱石油化工和RhÔne-Poulenc Agro (Bayer Crop Science)首次将吡草酮(Benzofenap)应用于商品化, 其商品名为“Yakawide”.由于结构的差异性, 相对于苄草酚, 吡草酮延长了其在土壤中的半衰期, 在同等剂量下吡草酮的药效时间可以增加至50 d, 而苄草酚的药效时间约为21~35 d; 同时吡草酮具有更好的作物选择性并且能够有效地避免高温致使其对水稻产生的短暂的药害现象.具体的合成路线如Scheme 2.
苯吡唑草酮(Topramezone)是由德国巴斯夫公司开发的玉米田除草剂. 2006年, 在北美洲和欧洲同时上市, 其商品名分别为“Impact”和“Clio”.在推荐使用剂量50~75 g ai/ha的条件下, 它能够有效的防治一年生玉米田中多种阔叶杂草和禾本科杂草, 相对于硝磺草酮、磺草酮, 其对狗尾草、马齿苋、马唐等杂草的防效几乎可以达到百分之百.同时, 与其他类的除草剂如二甲酚草胺、烟嘧磺隆制成混剂, 可有效拓宽杀草谱; 与三嗪类除草剂或麦草畏制成混剂几乎可以防治所有种属的阔叶杂草.目前, 苯吡唑草酮是玉米田最为安全、高效的HPPD类除草剂; 其几乎对所有品种的玉米都表现出高度安全性.工业可能的合成路线如Scheme 3, 以2, 3-二甲基硝基苯(Ⅱ-2a)为起始原料, 经过与亚硝酸丁酯反应得到安息香醛肟Ⅱ-2b, Ⅱ-2b经过氯化再与乙烯反应得到含异噁唑结构的中间体Ⅱ-2d.再经过后续的硝基还原反应、氨基甲硫基化、溴化、氧化以及偶联反应即能制备苯吡唑草酮[30].
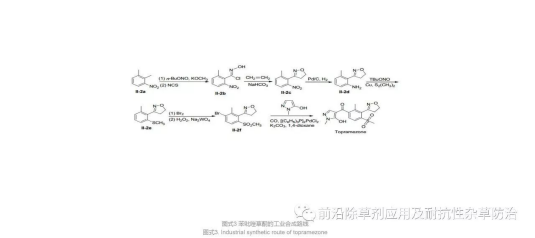
图式3苯吡唑草酮的工业合成路线
未完待续,下期奉献完整内容
来源:前沿除草剂应用及耐抗性杂草防治