Rimisoxafen是富美实公司(FMC)研究开发的兼具嘧啶和异唑结构新型苯联异唑类除草剂,于2021年3月获得ISO通用名,CAS登录号:1801862-02-1,化学名称:3-氯-2-(3-(二氟甲基)异唑-5-基)苯基5-氯嘧啶-2-基醚。化学结构式如图1。
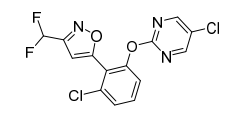
图1 Rimisoxafen化学结构式
rimisoxafen具有新颖双重除草作用机制,不仅可以通过抑制SDPS以损害光合作用,导致植物褪绿并最终死亡实现除草,还可以通过阻断PDS以耗尽类胡萝卜素,导致叶片白化、植物组织发生光氧化破坏实现除草。rimisoxafen可用于玉米、大豆等作物防除杂草,对稗草、黑草、猪殃殃、巨狐尾草、地肤、野苋菜、繁缕、藜、牵牛花、大马塘草、绒毛叶和苋菜藤子等单子叶杂草和阔叶杂草都具有优异防控效果,尤其对抗性苋属植物特别有效,市场前景十分广阔。
rimisoxafen合成路线主要有2条:
路线1:在异丙醇溶剂中,在碳酸钾存在条件下,3-氯-2-(3-(二氟甲基)异唑-5-基)苯酚与2,5-二氯嘧啶缩合得到rimisoxafen,合成路线见图2。
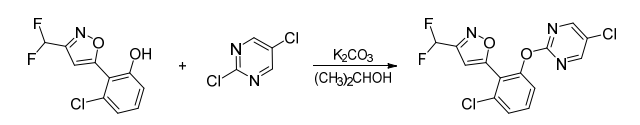
图2 rimisoxafen合成路线1
据文献报道,基于该路线合成rimisoxafen,收率低,难以实现工业化应用。
路线2:在异丙醇溶剂中,在碳酸钾存在条件下,3-氯-2-(3-(二氟甲基)异唑-5-基)苯酚与5-氯-2-(甲基磺酰基)嘧啶缩合得到rimisoxafen,合成路线见图3。
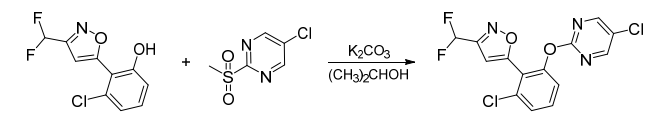
图3 rimisoxafen合成路线2
由于5-氯-2-(甲基磺酰基)嘧啶中的甲基磺酰基是一个很好的离去基团,具有较高的反应活性,基于该路线合成rimisoxafen,其收率高,反应条件温和,适于工业化生产应用。
基于以上反应路线,本文设计了5-氯-2-(甲基磺酰基)嘧啶的合成路线。以氯乙酰氯为原料,在草酰氯的作用下与N,N-二甲基甲酰胺反应,得到2-氯-3-(二甲氨基)-N,N-二甲基丙烯氯化胺,再与S-甲基异硫脲半硫酸盐成环,过氧化氢氧化得到中间体5-氯-2-(甲基磺酰基)嘧啶,合成路线见图4。
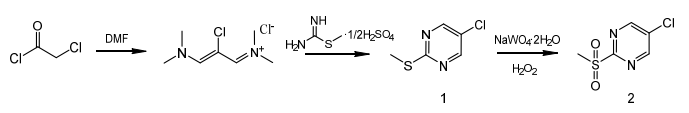
图4 5-氯-2-(甲基磺酰基)嘧啶合成路线
以2,6-二氯苯甲醛为起始原料,经甲基氯化镁格式反应,高锰酸钾氧化生成2',6'-二氯苯乙酮;然后与二氟乙酸乙酯反应得到5-氯-2-(二氟甲基)-4H-苯并吡喃-4-酮,最后和盐酸羟胺环化得到中间体3-氯-2-(3-(二氟甲基)异唑-5-基)苯酚;在异丙醇溶剂中,在碳酸钾存在条件下,3-氯-2-(3-(二氟甲基)异唑-5-基)苯酚与5-氯-2-(甲基磺酰基)嘧啶醚化,合成目标物质rimisoxafen,合成路线见图5。
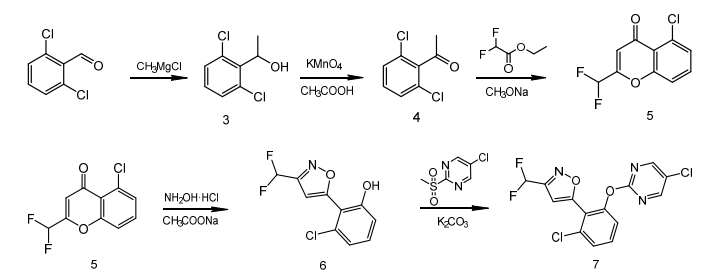
图5 rimisoxafen合成路线
实验部分
1. 主要仪器与试剂
400MR核磁共振波谱仪(安捷伦科技有限公司)、旋转蒸发器、循环水式多用真空泵(科贝科技股份有限公司)。
2,6-二氯苯甲醛(≥98.0%,希恩思化学试剂有限公司),氯乙酰氯(≥98.0%)、S-甲基异硫脲半硫酸盐(≥98.0%,麦克林生化科技有限公司),甲基氯化镁[3.0M THF(四氢呋喃),安耐吉化学试剂有限公司],盐酸羟胺(≥99.0%,武汉格奥恒晟科技发展有限公司),所用溶剂均为工业级。
2. 合成方法
5-氯-2-(甲硫基)嘧啶(1)的合成
5-氯-2-(甲基磺酰基)嘧啶(2)的合成
1-(2,6-二氯苯基)乙醇(3)的合成
2',6'-二氯苯乙酮(4)的合成
5-氯-2-(二氟甲基)-4H-苯并吡喃-4-酮(5)的合成
3-氯-2-(3-(二氟甲基)异唑-5-基)苯酚(6)的合成
rimisoxafen(7)的合成
...
结果与讨论
1. rimisoxafen的核磁共振氢谱( 1H NMR)结构表征确证
对rimisoxafen进行了核磁共振氢谱表征,谱图见图6。
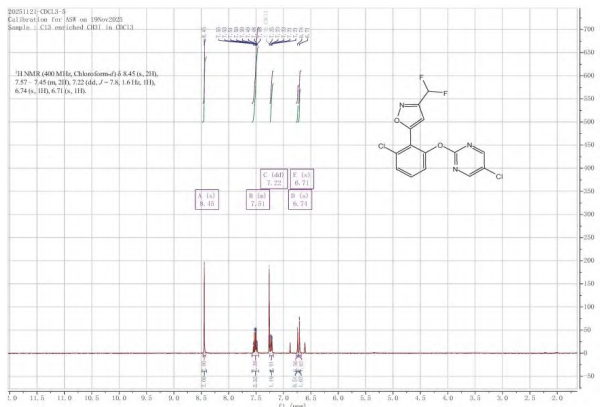
图6 rimisoxafen的1H NMR谱图
从1H NMR(400 MHz,CDCl3)谱图可知:6.71 ppm单峰为异唑-4-氢;6.74ppm三重峰为二氟甲基(CHF2)氢,该氢受其中F2影响裂分为三重峰;7.22~7.57ppm多重峰为苯环3个氢;8.45ppm单峰为嘧啶-4,6-2个氢;7.25ppm单峰为未氘代溶剂峰。上述谱图表征进一步确证rimisoxafen的结构。
2. 5-氯-2-(甲硫基)嘧啶的合成
5-氯-2-(甲硫基)嘧啶的合成过程中,N,N-二甲基甲酰胺先与氯化试剂反应,形成强亲电Vilsmeier中间体,再与S-甲基异硫脲半硫酸盐反应获得5-氯-2-(甲硫基)嘧啶。生成Vilsmeier中间体所需要的氯化试剂种类和用量是影响本反应重要因素。
氯化试剂的选择
反应常用的氯化试剂有二氯亚砜、三氯氧磷、草酰氯等。二氯亚砜与N,N-二甲基甲酰胺反应可以生成Vilsmeier中间体,但中间体过于活泼、不稳定,难以控制;三氯氧磷和N,N-二甲基甲酰胺反应生成Vilsmeier中间体,对温度和加料顺序要求较高,不便操作;草酰氯与N,N-二甲基甲酰胺反应生成Vilsmeier中间体,反应条件温和,便于操作。结合反应条件、反应后处理等因素选择草酰氯作为本反应的氯化试剂。
氯化试剂的用量对反应的影响
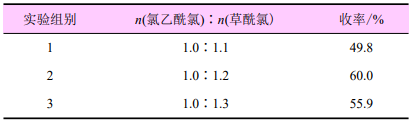
由表1可知:草酰氯与氯乙酰氯的摩尔比为1.2∶1.0时,收率最高,为60.0%,增加草酰氯的用量,收率基本无变化。故氯化试剂草酰氯与氯乙酰氯的摩尔用量为1.2∶1.0。
表1 草酰氯的用量对反应收率的影响
3. rimisoxafen的合成
在进行醚化过程中,酚羟基在碱的作用下,作为亲核试剂进攻5-氯-2-(甲基磺酰基)嘧啶并且中和离去的甲基磺酰基基团,使反应顺利进行。碱的种类及其使用量对反应有着明显影响。
碱的选择
常用碱有甲醇钠、乙醇钠、三乙胺、氢氧化钠、碳酸盐类等,本文选用了碱性较强的无水碳酸钾,既可以达到实验目的,又降低了成本。故选择碳酸钾作为碱。
碱用量对反应的影响
参考上述rimisoxafen(7)的合成方法,在其他条件不变的情况下,探究了碳酸钾用量对反应的影响,结果见表2。由表2可知:3-氯-2-(3-(二氟甲基)异唑-5-基)苯酚与碳酸钾的摩尔比为1.0∶1.5时,收率最高,为81.6%,增加碳酸钾的用量,收率基本无变化。故碳酸钾与3-氯-2-(3-(二氟甲基)异唑-5-基)苯酚的摩尔用量为1.5∶1.0。
表2 碳酸钾的用量对反应收率的影响

反应时间对rimisoxafen收率的影响
在3-氯-2-(3-(二氟甲基)异唑-5-基)苯酚与碳酸钾的摩尔比为1.0∶1.5,反应温度为65℃的条件下,考察了反应时间对产物收率的影响,结果见表3。
表3 反应时间对反应收率的影响
结果表明:反应2h即可进行完全。缩短反应时间,反应不彻底;延长反应时间,产率基本无变化。最佳反应时间为2h。
结论
基于rimisoxafen文献报道合成工艺,以氯乙酰氯为原料,在草酰氯的作用下依次与N,N-二甲基甲酰胺、S-甲基异硫脲半硫酸盐反应成嘧啶环,再氧化得到中间体5-氯-2-(甲基磺酰基)嘧啶;以2,6-二氯苯甲醛为起始原料,经格式反应、氧化反应生成2',6'-二氯苯乙酮,再与二氟乙酸乙酯反应得到5-氯-2-(二氟甲基)-4H-苯并吡喃-4-酮,最后和盐酸羟胺环化得到中间体3-氯-2-(3-(二氟甲基)异唑-5-基)苯酚。在异丙醇溶剂中,在碳酸钾存在条件下,5-氯-2-(甲基磺酰基)嘧啶与3-氯-2-(3-(二氟甲基)异唑-5-基)苯酚醚化合成rimisoxafen。该工艺原料廉价易得,反应条件温和,适于工业化生产。
作者:刘安昌1; 刘家俊1; 敖承四1; 谢睿1; 程子涵1; 余磊2(1.武汉工程大学化工与制药学院 2.武汉软件工程职业学院(武汉开放大学))