芳基吡唑类杀虫剂具有高效、低毒等优点,与现代绿色农药的发展理念相吻合,因而在当前所开发农药新品种中,涌现出越来越多的芳基吡唑类杀虫剂、杀螨剂,例如氟虫腈(fipronil)、乙虫腈(ethiprole)、丁虫腈(flufiprole)等。然而,由于长期大量的不合理使用,目前多种农业害虫如小菜蛾、烟粉虱、稻飞虱、二化螟、斜纹夜蛾和棉铃虫等对传统的芳基吡唑类杀虫剂已产生了严重抗药性。因此,开发新型、高效的芳基吡唑类杀虫、杀螨剂已迫在眉睫。
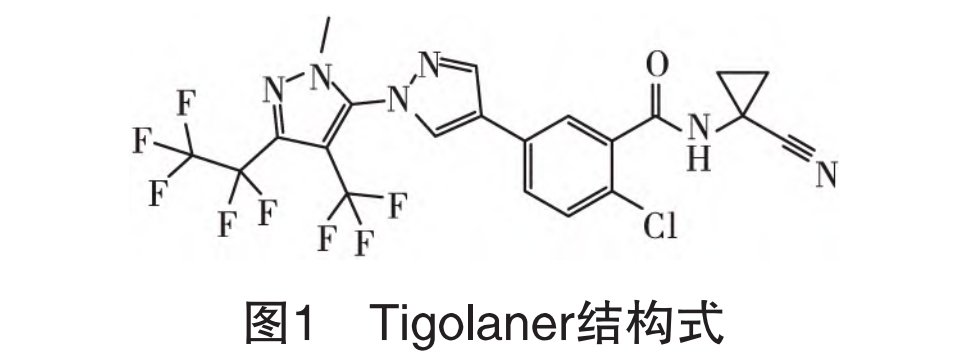
Tigolaner是由德国Bayer公司研发的新型芳基吡唑类杀虫杀螨剂,CAS登录号为1621436-41-6,分子式为C21H13ClF8N6O,相对分子质量为552.81,其IUPAC名称为2-氯-N-(1-氰基环丙基)-5-[1-[2-甲基-5-(1,1,2,2,2-五氟乙基)-4-三氟甲基吡唑-3-基]吡唑-4-基]苯甲酰胺,结构式见图1。
该物质属于γ-氨基丁酸(GABA)受体非竞争性拮抗剂(non-competitive antagonists,NCAs),与传统的芳基吡唑类杀虫剂(如氟虫腈)及其他现有杀虫剂无交互抗性。其作用机制是通过与昆虫神经系统中的GABA受体结合,阻滞神经细胞的氯离子通道,抑制氯离子内流,进而破坏其神经系统的正常功能,引起神经和肌肉的过度兴奋,最终导致昆虫抽搐死亡。
目前,tigolaner已被应用于动物保健领域。法国Vetoquinol公司在2021年推出的猫用驱虫剂产品FelprevaR,是第一个以tigolaner为主要成分的商品化兽药,可用于跳蚤、蜱虫、蛔虫、绦虫和耳螨等寄生虫的感染,该产品也是欧盟批准的第一个针对猫的滴剂驱虫药。有报道称,样本患猫在使用该产品28 d后,其粪便中的肠道线虫和肺蠕虫的幼虫(含虫卵)总数分别减少了97.47%和96.80%,且用药期间无不良反应,是一款有效性和安全性俱佳的兽药产品。
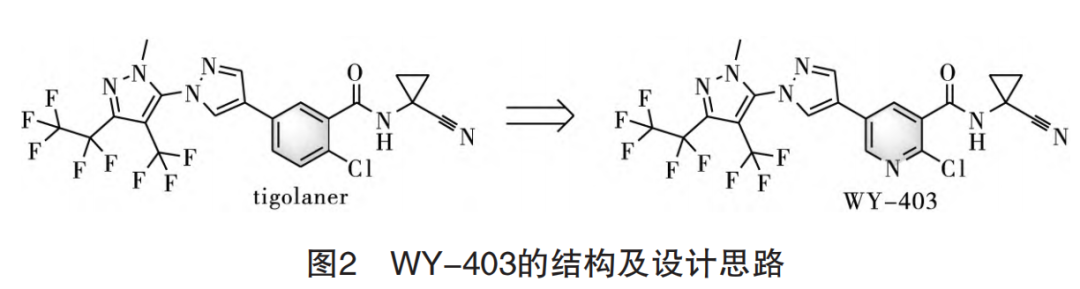
除已知物tigolaner外,本实验还选取了其类似物WY-403(见图2)。WY-403是将tigolaner分子中的苯环结构替换为吡啶环而得到,期望吡啶环上的氮原子可以作为氢键受体增强药物分子与受体蛋白之间的亲和力,进而增强药物的杀虫活性。实验以全氟-4-甲基-2-戊烯为原料,经过4步反应制备得到了这2个化合物。
在温室条件下测试了2者对农业害虫小菜蛾、朱砂叶螨及桃蚜的杀虫杀螨活性。同时,为了探究药物分子配体与靶标受体蛋白之间的结合模式,采用同源模建的方法,以秀丽隐杆线虫谷氨酸门控性氯离子通道受体蛋白的晶体结构为模板构建了果蝇RDL受体蛋白模型,然后将tigolaner和WY-403与所建模型进行了分子对接,研究2个化合物与受体的结合模式,并以此判断WY-403对靶蛋白是否有更强的亲和力,旨在为后续tigolaner及其类似物在农业害虫防治领域提供新的应用方向、研发方向及理论支撑。
1. 材料
全氟-4-甲基-2-戊烯,纯度97%,安徽泽升科技有限公司;氟化铯(CsF),分析纯,上海迈瑞尔生化科技有限公司;乙腈(MeCN),分析纯,天津市大茂化学试剂厂;三乙胺(TEA)、异丙醇(i-PrOH)、N,N-二甲基甲酰胺(DMF),分析纯,天津市富宇精细化工有限公司;二氯甲烷(DCM),分析纯,永华化学股份有限公司;4-吡唑硼酸频哪醇酯,纯度97%,天津希恩思生化科技有限公司;碳酸钾(K2CO3)、碳酸氢钠(NaHCO3),分析纯,天津市恒兴化学试剂制造有限公司;5-溴-2-氯苯甲酸、5-溴-2-氯烟酸,纯度98%,上海皓鸿生物医药科技有限公司;氯化亚砜(SOCl2),化学纯,上海麦克林生化科技股份有限公司;甲苯、三氯甲烷,分析纯,辽宁泉瑞试剂有限公司;1-氨基环丙基腈盐酸盐,纯度97%,上海毕得医药科技股份有限公司;N,N-二异丙基乙胺(DIPEA),分析纯,上海阿拉丁生化科技股份有限公司;四(三苯基膦)钯[Pd(PPh3)4],分析纯,陕西瑞科新材料股份有限公司。
2. 分析测试仪器
AVANCE III 600 MHz核磁共振波谱仪,瑞士布鲁克公司;Accurate-Mass Q-TOF LC-MS液质联用仪,美国安捷伦公司;CHEETAH中压快速纯化制备色谱,天津博纳艾杰尔科技有限公司;N-1300型旋转蒸发仪,东京理化器械株式会社;MP450全自动熔点仪,济南海能仪器股份有限公司。
3. 化合物的合成
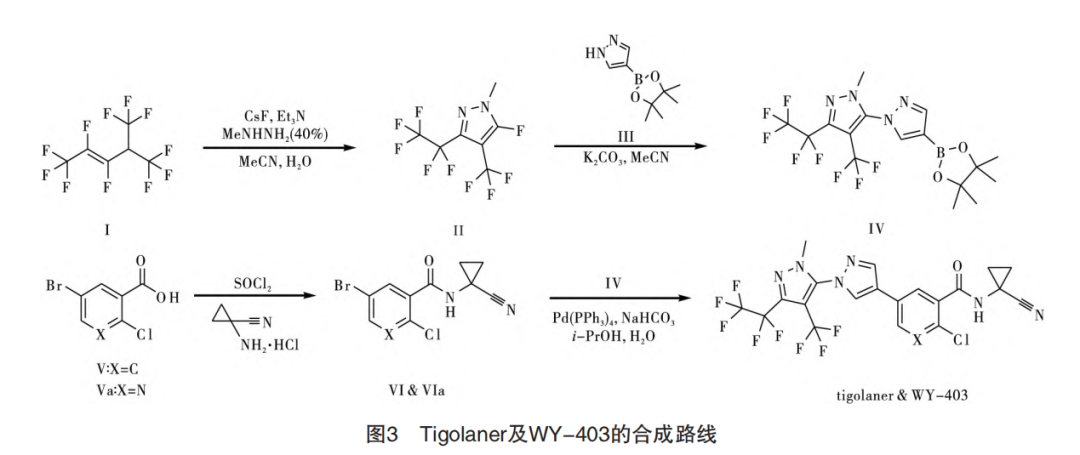
通过文献调研,本实验采用了如下合成路线,见图3。
(1)5-氟-1-甲基-3-(全氟乙基)-4-(三氟甲基)-1H-吡唑(Ⅱ)的合成
在一个500 mL三口瓶中加入全氟-4-甲基-2-戊烯(I)24.8 g(82.7 mmol)、氟化铯258 mg(1.7 mmol)和乙腈165 mL,将其置于50 ℃下反应8 h,然后把混合物冷却至室温,加入水2 mL。将混合物冷却至0 ℃,然后向瓶内缓慢滴入三乙胺20.9 g(206.6 mmol),滴加过程中保持温度在0~5 ℃。滴毕,使混合物维持在0 ℃下搅拌20 min,然后向瓶中缓慢滴加40%的N-甲基肼水溶液10.0 g(86.8 mmol),滴加过程中也保持温度在0~5 ℃。滴毕,将反应瓶移至室温下继续搅拌20 h。
搅拌结束后,在减压(0.05 MPa)下蒸除溶剂,用二氯甲烷溶解残留物,加水洗涤,用无水硫酸钠干燥有机相,并在常压下浓缩,得到22.7 g红褐色液体Ⅱ,收率95.9%。所得粗品未经继续纯化直接用于下一步。
(2)2'-甲基-5'-(全氟乙基)-4-(4,4,5,5-四甲基-1,3,2-二氧杂硼烷-2-基)-4'-(三氟甲基)-2'H-1,3'-联吡唑(Ⅳ)的合成
向一个500 mL单口瓶中加入4-吡唑硼酸频哪醇酯(Ⅲ)15.4 g(79.3 mmol)和乙腈160 mL,再加入碳酸钾粉末16.4 g(118.9 mmol)和中间体Ⅱ 22.7 g(79.3 mmol)。将混合物回流搅拌7 h然后冷却至室温。冷却之后将反应混合物过滤,用乙腈30 mL洗涤滤饼,并把合并的滤液蒸干。用异丙醇60 mL溶解蒸干后的残余物,溶解之后向瓶内加水
300 mL,再将混合物冷却至3 ℃,滤出沉淀。将固体用水洗涤并烘干,得到25.9 g淡黄色固体Ⅳ,收率71.2%。
1H NMR(600 MHz,CDCl3) δ:8.08(s,1H),7.93(s,1H),3.77(s,3H),1.35(s,12H)。
(3)中间体Ⅵ和Ⅵa的合成
向一个250 mL单口瓶中,加入5-溴-2-氯苯甲酸(V)15 g(63.7 mmol)、N,N-二甲基甲酰胺95 mg(1.3 mmol)、甲苯70 mL和氯化亚砜22.7 g(191 mmol)。将混合物在105℃下加热1 h后冷却至室温,蒸除溶剂和过量的氯化亚砜。把残余物溶解在40 mL三氯甲烷中,将其缓慢滴加到1-氨基环丙基腈盐酸盐11.3 g(95.3 mmol)、N,N-二异丙基乙胺28.7 g(221.9 mmol)和三氯甲烷150 mL的混合悬浮液中,使其在室温下搅拌过夜。向混合液中加入饱和碳酸氢钠水溶液,搅拌30 min后过滤,收集滤饼。
将滤液中的有机相分出,并用无水硫酸钠干燥后浓缩,残留物用少量三氯甲烷打浆后过滤,再次收集滤饼。将2次所得的滤饼合并,用水漂洗并烘干,得到17.5 g白色固体Ⅵ。中间体VIa可由5-溴-2-氯烟酸(Ⅴa)经类似的方法制得。
5-溴-2-氯-N-(1-氰基环丙基)苯甲酰胺(Ⅵ):白色固体,收率91.7%,m.p. 179.0~180.9 ℃。1H NMR(600 MHz,DMSO) δ:9.46(s,1H),7.72(d,J=2.4 Hz,1H),7.69(dd,J=8.6,2.5 Hz,1H),7.49 (d,J=8.6 Hz,1H),1.58~1.55(m,2H),1.30~1.27(m,2H)。ESI-MS, m/z:[M+Na]+理论值320.94,测试值320.92。
5-溴-2-氯-N-(1-氰基环丙基)烟酰胺(Ⅵa):白色固体,收率93.4%,m.p. 181.1~183.0 ℃。1H NMR(600 MHz,DMSO) δ:9.58(s,1H),8.69(d,J=2.4 Hz,1H),8.33 (d,J=2.5 Hz,1H),1.60~1.58(m,2H),1.30~1.28(m,2H)。ESI-MS,m/z:[M+Na]+理论值321.94,测试值321.90。
(4)Tigolaner及WY-403的合成
向一个500 mL单口瓶中加入中间体Ⅳ9.6 g(20.9 mmol)、异丙醇(160 mL)和水(32 mL),再向其中加入中间体Ⅵ 6.3 g(20.9 mmol),碳酸氢钠5.3 g(62.7 mmol),最后向其中加入四(三苯基膦)钯1.2 g(418 μmol),将混合物在氮气氛围下换气3次后回流加热5 h。将反应混合物过滤,然后用异丙醇(40 mL)洗涤滤饼,并把滤液浓缩蒸干。向残留物中加入异丙醇(80 mL)和水(200 mL),充分搅拌使产物析出,然后抽滤出固体,用少量水洗涤滤饼,烘干可得10.7 g白色固体tigolaner。WY-403可由中间体Ⅳ与中间体Ⅵa经类似的方法制得。
Tigolaner:白色固体,收率92.8%,m.p. 203.4 ~204.4 ℃;1H NMR (600 MHz,CD3CN ) δ:8.27 (s,1H),8.25 (s,1H),7.74(d,J=2.3 Hz,1H),7.70(dd,J=8.4,2.3 Hz,1H),7.57(brs,1H),7.51(d,J=8.4 Hz,1H),3.75(s,3H),1.59~1.57(m,2H),1.36~1.34(m,2H);13C NMR(151 MHz,CDCl3) δ:166.71,141.14,138.33(d,J=3.4 Hz),137.35(t,J=30.8 Hz),133.79,131.09,130.20,129.92,129.59,129.29,127.88,123.62,120.31(q,J=268.9 Hz),119.70,118.45(qt,J=286.9,36.4 Hz),109.86 (tq,J=253.2,39.9 Hz),107.77 (q,J=39.8 Hz),37.59,20.92,17.02。ESI-HRMS,m/z:[M+Na]+理论值575.0609,测试值575.0616。
WY-403:白色固体,收率94.6%,m.p. 205.7~206.5 ℃;1H NMR(600 MHz,CD3CN) δ:8.74(d,J=2.5 Hz,1H),8.32(s,1H),8.31(s,1H),8.12(d,J=2.4 Hz,1H),7.67(brs,1H),3.76(s,3H),1.61~1.59(m,2H),1.37~1.34(m,2H);13C NMR(151 MHz,CDCl3) δ:165.33,148.32,145.62,141.05,138.06(d,J=3.4 Hz),137.47 (t,J=31.5 Hz),136.99,130.53,129.91,126.73,120.28 (q,J=268.7 Hz),120.16,119.55,118.45(qt,J=286.6,36.6 Hz),109.85(tq,J=253.3,39.8 Hz),107.96(q,J=40.3 Hz),37.68,21.04,17.00。ESI-HRMS,m/z:[M+Na]+理论值576.0562,测试值576.0566。
4. 生物活性测试
(1)对小菜蛾的生物活性
取3 mg原药,用3 mL丙酮-甲醇(体积比1∶1,下同)混合溶剂溶解,然后用含有0.2%(质量分数,下同)吐温80的精制自来水稀释成系列质量浓度。以同样方法设置四氯虫酰胺(tetrachlorantraniliprole)的对照试验组,另设清水为空白对照。
采用Airbrush喷雾法,用打孔器将新鲜干净的甘蓝叶片制成直径3.0 cm的叶碟,再用Airbrush喷雾机按质量浓度由低到高顺序对叶碟均匀喷雾,然后放入垫有滤纸的培养皿中自然阴干。接入10头供试小菜蛾,置于培养箱中饲养,48 h后进行试验调查,记录试虫的死虫与活虫数。设置3次重复,结果取平均值。致死率按式(1)进行计算。
(2)对朱砂叶螨的生物活性
取3 mg原药,用3 mL丙酮-甲醇溶解,然后用含有0.2%吐温80的精制自来水稀释成系列质量浓度,以同样方法设置乙唑螨腈(cyetpyrafen)和阿维菌素(abamectin)的对照试验组,另设清水为空白对照。摘取2片温室真叶菜豆苗,接种朱砂叶螨成螨并调查基数后,用手持喷雾器进行整株喷雾处理,试验设置3次重复,处理后置于标准观察室,48 h后调查存活螨数,致死率按式(1)计算。
(3)对桃蚜的生物活性
取3 mg原药,用3 mL丙酮-甲醇溶解,然后用含有0.2%吐温80的精制自来水稀释成系列浓度,以同样方法设置吡虫啉的对照试验组,另设清水为空白对照。采用Airbrush喷雾法,从培养桃蚜的甘蓝植株上剪取大小适宜(直径约3 cm)且长有15~30头蚜虫的甘蓝叶片,用Airbrush喷雾机按浓度由低到高顺序对叶碟正反面均匀喷雾,待叶片自然阴干后,移至标准观察室中观察,试验设置3次重复,48 h后记录试虫的死虫与活虫数,致死率按式(1)计算。
5. 药物分子与目标蛋白的相互作用模式研究
Tigolaner和WY-403的作用对象是昆虫体内的GABA受体,该受体是昆虫神经系统中主要的抑制性神经递质受体,是林丹(gamma-HCH)、毒杀芬(camphechlor)、氟虫腈以及阿维菌素等多种杀虫剂的作用靶标,其结构与哺乳动物GABAA离子型受体相似,2者都是半胱氨酸环受体(Cys-loop receptor)超家族中的成员,该家族还包括烟碱乙酰胆碱受体(nAChR)、甘氨酸受体(GlyR)、谷氨酸受体(GluR)及5-羟色胺3受体(5-HT3R)等。
GABA受体是跨膜蛋白,是由5个亚基组装而成的五聚体,见图4(a),每个亚基都包含1个较长的N端胞外结构域、4个高度保守且联系密切的跨膜结构域(transmembranedomains, TM1~TM4)及1个连接TM3和TM4的大环胞内结构域见图4(b)。
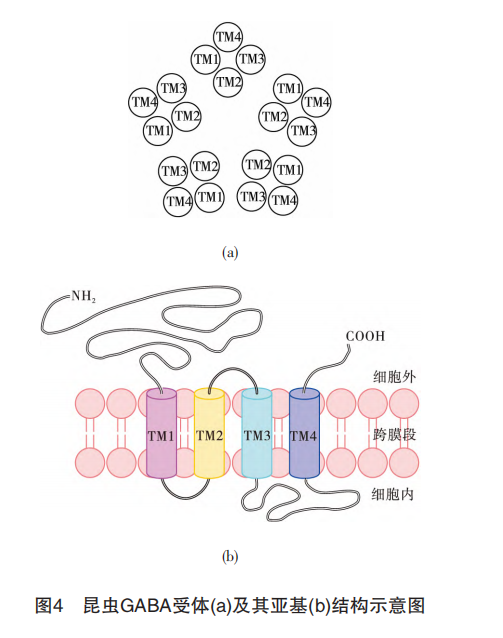
其内源性配体GABA的结合位点位于亲水的胞外区,而NCAs的作用位点则多位于5个TM2螺旋包围的氯离子通道孔中。由于昆虫的GABA受体研究不多,目前仅有3种昆虫的GABA受体亚基被报道,分别是RDL(resistance to dieldrin)、LCCH3 (ligand -gated chloride channel homologue 3)和GRD(GABA and glycine-like receptor of Drosoplila),而这3种亚基之中只有RDL亚基被证明能够在GABA的突触传递及视觉和嗅觉过程中起作用,因此昆虫GABA受体也被称为RDL受体。
(1)同源模建
由于目前还未见到有关昆虫GABA受体晶体结构的相关文献报道,故需利用同源模建的方法构建昆虫GABA受体蛋白的三维模型。
从UniprotKB数据库中获得果蝇的RDL亚基序列(登录号:P25123),将其作为目标序列。在RSCB PDB数据库中选取秀丽隐杆线虫谷氨酸门控性氯离子通道蛋白(GluCl)(PDB ID: 3RHW,分辨率:3.26魡)为模板蛋白,构建昆虫GABA受体的蛋白模型,目前已有利用GluCl构建昆虫GABA受体的文献报道。使用ClustalW2程序将目标亚基序列与模板序列与进行比对生成MSF文件。在SYBYL-X 2.1软件的ORCHESTRAR模块中导入MSF文件分别完成对5个亚基的构建,再通过Edit/Merge模块将构建好的亚基与模板受体叠合组成五聚体,并用AMBER力场对生成的五聚体模型进行能量最小化。最后,使用PROCHECK对得到的五聚体模型进行验证。
(2)分子对接
使用AutoDock 4.2.6软件对小分子化合物与所建模型进行虚拟对接计算。先对靶蛋白和小分子分别进行加氢、添加原子类型、计算电荷等一系列预处理,再确定对接盒子,而后将小分子放入对接盒子中进行构象搜索,最后根据结合能、氢键数等评价指标评价对接效果。使用Discovery studio 2021 Client软件绘制对接结果的2D、3D效果图。
1. 生测结果
Tigolaner及WY-403的杀虫活性结果见表1。
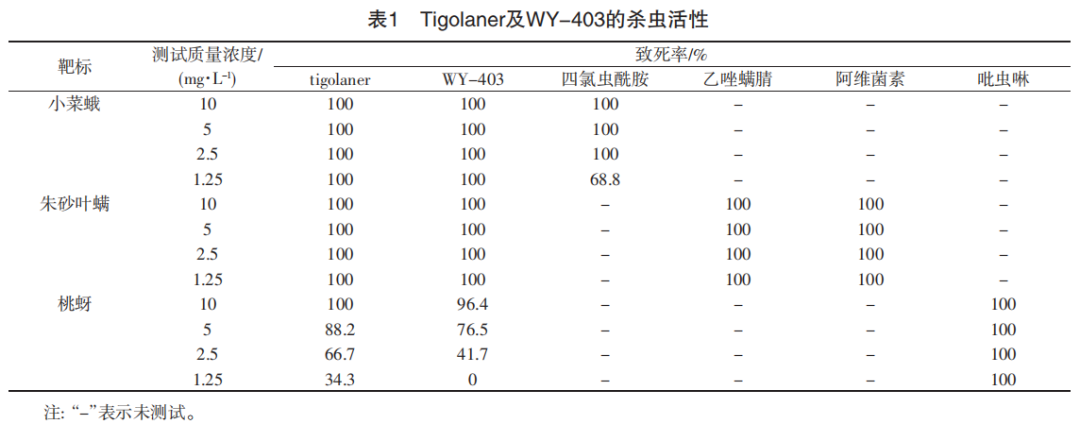
由表1数据可知:在10、5、2.5、1.25 mg/L质量浓度下,tigolaner及WY-403对小菜蛾致死率均为100%,优于对照药剂四氯虫酰胺;2者在测试质量浓度下对朱砂叶螨的致死率同样可达100%,与对照药剂乙唑螨腈和阿维菌素相当;在10 mg/L质量浓度下,tigolaner和WY-403对桃蚜也能达到100%和96.4%的高致死率,2者对桃蚜的LC50值分别在1.25~2.5 mg/L(tigolaner)和2.5~5 mg/L(WY-403)范围内,虽略逊于对照药剂吡虫啉,但也表现出了不错的杀虫活性。整体来看,tigolaner和WY-403杀虫活性相当,2者都具有优秀而广谱的杀虫活性。
2. 相互作用模式研究结果
(1)蛋白模型的合理性评价
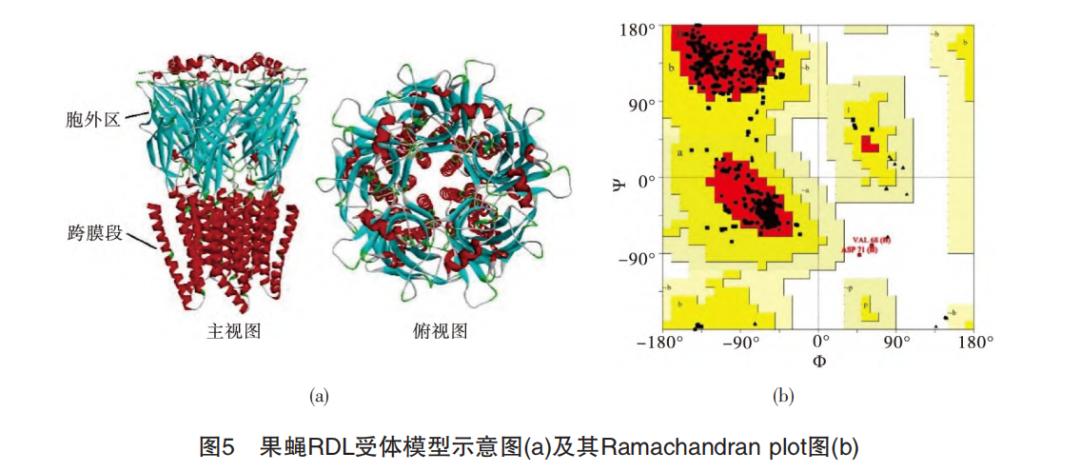
通过同源模建得到的果蝇RDL受体的三维结构模型如图5(a)所示,利用PROCHECK程序对所建模型进行评价,通过生成的Ramachandran plot图来检测蛋白主链中氨基酸残基Φ-Ψ二面角的合理性,如图5(b)所示。分析得出,大量氨基酸残基位于Φ=-57°、Ψ=-47°处,表明受体结构中有较多α螺旋的结构特征;还有些氨基酸分散在Φ=-135°、Ψ=135°附近,表明受体结构中也存在一些β-折叠的结构特征。
结合图5(a),果蝇RDL受体蛋白胞外区结构以β-折叠(蓝绿色)为主,跨膜段则是以α-螺旋(红色)为主,这与Ramachandran plot图反映的信息相吻合。
此外,从图5(b)中还可以看出:有91.0%的氨基酸残基落在了核心区域,8.6%的氨基酸落在了合理区域,仅有0.4%的氨基酸残基(如ASP71、VAL68等)落在了不合理区域。将目标蛋白与模板蛋白的三维结构进行叠合分析,ASP71、VAL68等氨基酸残基均位于胞外区,与受体蛋白的结合口袋相距很远,对后续研究药物分子与受体蛋白的结合模式不会带来影响。以上信息都反映出所建模型的合理性。
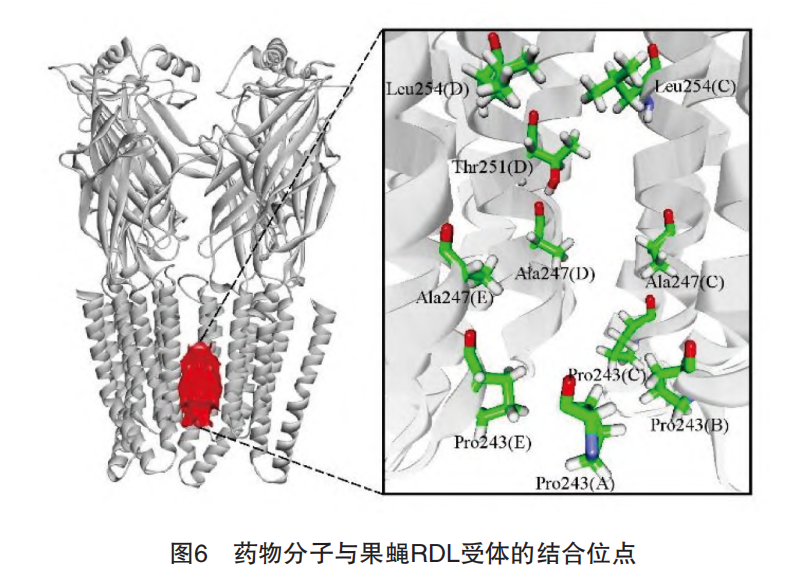
(2)对接位点
只有确定好参与对接的关键氨基酸残基,才能定义好药物分子与受体的结合口袋。据已有文献报道,在果蝇RDL同源五聚体中,位于TM2螺旋上的2′Ala、6′Thr和9′Leu与多种NCAs的结合起关键性作用,如图6所示。据此可利用AutoDock 4.2.6软件中的Grid模块设置出囊括这些关键氨基酸的对接盒子,其中心坐标为13.158、114.059、35.871(x,y,z),盒子大小为18魡×26魡×20魡。
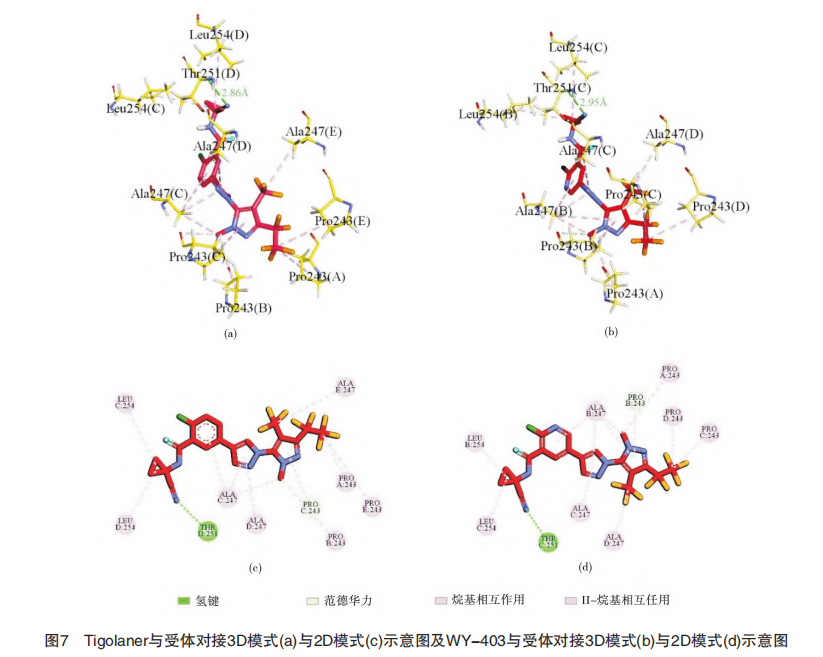
(3)分子对接结果
Tigolaner及WY-403与果蝇RDL受体的结合能分别为-9.5、-9.2 kcal/mol。图7为2个化合物与果蝇RDL受体蛋白模型对接的2D、3D效果图。对接结果显示,2者在受体蛋白中的构象类似,都位于通道Pro243~Leu254的中间部分,氟代吡唑环朝向胞内区,氰基环丙基朝向胞外区一端。
2分子的全氟乙基、三氟甲基、环丙基及芳环结构均与周围的氨基酸残基存在不同程度的疏水相互作用,而氰基则与受体中的Thr251形成长度分别为2.86魡和2.95魡的氢键,氢键的长度小于3魡表明氢键具有良好的强度和稳定性。这些相互作用使配体分子与果蝇RDL受体形成了稳定的复合物,这揭示了tigolaner和WY-403对害虫害螨具有优异防效的深层原因。
以全氟-4-甲基-2-戊烯为原料,经4步反应制得化合物tigolaner和WY-403,结构经1H NMR、13C NMR和ESIHRMS确认,反应条件温和、原料廉价易得,适合大规模制备。
生物活性测试结果表明:tigolaner和WY-403具有优异的杀虫杀螨活性。在测试质量浓度低至1.25 mg/L时,2个化合物对小菜蛾和朱砂叶螨的致死率仍能高达100%。在测试质量浓度为10 mg/L时,2个化合物对桃蚜的致死率也分别达到了100%和96.4%,杀虫活性优异。
以秀丽隐杆线虫谷氨酸门控性氯离子通道受体蛋白的晶体结构为模板构建了果蝇的RDL受体蛋白模型,其Ramachandran plot图表明所建模型合理。
Tigolaner和WY-403与果蝇RDL受体的分子对接结果表明:2个化合物与靶标受体蛋白之间存在着高亲和性,这是tigolaner与WY-403具有优异的杀虫杀螨活性的最根本原因,这为后续tigolaner及其类似物在农业害虫防治领域的应用提供了理论支撑。
作者:毕庆杰、刘东东、李泽东、罗春凤、张静、张立新
